الجهاز العصبي systema nervosum 
رسم توضيحي للجهاز العصبي في الإنسان بشقيه المركزي CNS (بالأحمر)، والمحيطي PNS (بالأزرق)
تفاصيل
يتكون من جهاز عصبي مركزي
، وجهاز عصبي محيطي
نوع من نظام أحيائي
الجهاز العصبي ويدعى أيضاً الجملة العصبية هو أهم الأجهزة التي تميز المملكة الحيوانية. يشاهد عند كل الكائنات الحية ابتداءً من وحيدات الخلايا وحتى الثدييات حيث يكون مؤلفاً من دارات بسيطة بين مجموعات صغيرة من خلايا عصبية عند وحيدات الخلايا، ويزداد تعقيداً كلما صعدنا في سلم التطور ليصل إلى أقصى درجات التعقيد والكفاءة عند الإنسان.
الجهاز العصبي هو شبكة اتصالات داخلية في جسم الكائن الحي تساعده على التواؤم مع التغييرات البيئية المحيطة به. ويمتلك كل كائن حي ـ ماعدا الحيوانات الأولية البسيطة ـ نوعًا من الأجهزة العصبية.
تمتلك الحيوانات اللافقارية جهازًا عصبيًا يتراوح بين شبكات بسيطة من الأعصاب وجهاز عصبي منظم مرتبط بدماغ بدائي. أما في الإنسان والحيوانات الفقارية، فيتكون الجهاز العصبي من دماغ ونُخاع شوكي وأعصاب. وتختص هذه المقالة بالجهاز العصبي في الإنسان.
يتميز الجهاز العصبي عند الإنسان بتطور الدماغ لدرجة مكنت من إنتاج اللغة و تطور وظائف الإدراك العليا مثل التعلم، الاستدلال المنطقي، التجريد، التخيل و الإبداع مما ساعده على التعامل مع التحديات بكفاءة عالية جداً.
وللجهاز العصبي في الإنسان عدة سُبل تُسهِّل انتقال المعلومات والإحساسات من البيئة المحيطة بالإنسان إلى الدماغ، الذي يقوم بإرسال أوامر وتعليمات لعضلات الجسم المختلفة، لتتجاوب مع تلك المعلومات. وتسلك هذه الأوامر سُبُلاً غير التي سلكتها المعلومات الواصلة للدماغ. وكذلك يختص الجهاز العصبي بتنظيم العديد من وظائف الجسم الداخلية، مثل عمليات التنفس والهضم والنبض القلبي. فالجهاز العصبي مسؤول عن كل ما يقوم به الإنسان من حركات وأفكار وانفعالات وأحاسيس.
يقوم الجهاز العصبي بوظيفته من خلال الاتصالات الكثيفة عبر المشابك العصبية الموجودة على نهايات محوار والتغصنات الهيولية العصبية لكل العصبونات التي تؤمن استقبال المعلومات، معالجتها، واصدار التعليمات.
يقوم الجهاز العصبي باستقبال المعلومات الواردة من المحيط الخارجي بواسطة أعضاء الإحساس ومن الأعضاء الداخلية بواسطة المستقبلات الحسية المنتشرة في المفاصل والعضلات والأحشاء، حيث تعالج تلك المعلومات بسرعة فائقة، ليصار إما إلى تخزينها كذاكرة وخبرة أو إصدار أوامر لأجهزة الجسم الأخرى بما يتناسب مع المعلومات الواردة.الخلية الرئيسية هي العصبون، أو ما يدعى بالخلية العصبية، التي تلعب دورا أساسيا في كل فعاليات الدماغ.
عندما تكون بعض الحيوانات مجردة من المكون الأساسي للجهاز العصبي والمسمى الدماغ، يكون الجهاز العصبي عاجزا عن تشكيل أفكار أو إظهار مشاعر. بالتالي يعتبر الدماغ بشكل خاص والجهاز العصبي عامة المسؤول عن "إحياء" (بث الحياة) في الحيوانات (بكل ما يميز هذه الحياة من فعاليات) (تعتبر الإسفنجيات استثناء في هذا المجال)، ولنفس السبب فإن المواد الكيميائية السمية التي تعطل عمل الجهاز العصبي تسبب سريعا الشلل من ثم الموت في أحيانا كثيرة.
الجهاز العصبي للحيوانات الفقارية يقسم عادة إلى جهاز عصبي مركزي وجهاز عصبي محيطي. الجهاز العصبي المركزي يتألف من الدماغ والنخاع الشوكي. في حين يتألف الجهاز العصبي المحيطي من جميع العصاب والعصبونات التي لا تقع ضمن نطاق الجهاز العصبي المركزي. الغالبية العظمى مما يدعى الأعصاب (وهي الامتدادات المحورية للخلايا العصبية) تعتبر من ضمن الجهاز العصبي المحيطي. يتم تقسيم الجهاز العصبي المحيطي عادة إلى جهاز عصبي جسدي وجهاز عصبي ذاتي.
الجهاز العصبي الجسدي هو المسؤول عن توجيه حركات الجهاز العصبي للجسم وأيضا استقبال المنبهات الخارجية. أما الذاتي فهو جزء مستقل يعمل على تنظيم الوظائف الداخلية للجسم.
====================
آلية عمل الجهاز العصبي
يتكون الجهاز العصبي من بلايين الخلايا المختصة التي تسمى العصبونات أو الخلايا العصبية، والتي تتجمع في شكل حبال تُسمى الأعصاب، تسلك سُبلاً متعددة تساعد على نقل المعلومات سريعاً إلى كل مكان من الجسم.
يشترك في إحداث رد فعل الإنسان لأي موقف، العديد من العمليات المعقّدة داخل الجهاز العصبي، والتي لاتستغرق سوى لحظة واحدة. فلنأخذ مثلاً ماذا يحدث في الجهاز العصبي للإنسان، عندما يُشاهد نمراً مفترساً، ثم في لحظة يُطلق ساقيه للريح؟.
توجد في كل عضو من أعضاء الحواس، مثل العين والأذن وغيرها، عصبونات متخصصة تُسمى المستقبلات، تقوم بترجمة ما يحسه الإنسان، كرؤيته نمراً مفترساً، إلى إشارات عصبية، تُسمى الدُفعات العصبية، التي تنتقل في الألياف العصبية بسرعة 1 - 90م في الثانية. فعند رؤية النمر تستجيب مُسْتَقْبلات العينين للإشعاعات الضوئية، التي تعكس رؤيته وتترجمها إلى دفعات عصبية، تنتقل عبر عَصْبونات حسية من المستقبلات في أعضاء الحواس إلى عَصْبونات الترابط الموجودة في الدماغ والنخاع الشوكي.
تستقبل العَصْبونات في الدماغ الدفعات العصبية وتقوم بتحليلها وترجمتها وتقرر ما يجب اتخاذه حيالها. فمثلاً تترجم رسالة رؤية النمر المفترس إلى الشعور بالخوف، ومن ثَمّ يرسل الدماغ دُفعات عصبية أخرى، تنتقل عبر عَصْبونات حركية إلى المستفعلات، مثل العضلات والغدد التي تستجيب لأوامر الدماغ. فمثلاً تستجيب عضلات الساقين، وتساعد الإنسان على العدو بعيدًا عن الخطر. وكذلك يرسل الدماغ رسالة إلى القلب ليسرع من نبضه ويزيد من انقباضاته، ليرسل مزيدًا من الدم إلى عضلات الساقين.
أقسام الجهاز العصبي
يتكون الجهاز العصبي من قسمين رئيسيين هما: الجهاز العصبي المركزي والجهاز العصبي المحيطي. كل منهما مسؤول عن وظائف معينة.
تصغير
الجهاز العصبي المركزي مقالة مفصلة: الجهاز العصبي المركزي
مقالة مفصلة: الجهاز العصبي المركزي
يتكون الجهاز العصبي المركزي من الدماغ والنخاع الشوكي ويقوم بتنظيم جميع أنشطة الجهاز العصبي والتحكم فيها. والدماغ عضو شديد التعقيد، يتكون من ثلاثة أجزاء أساسية هي: المخ والمخيخ وجذع الدماغ.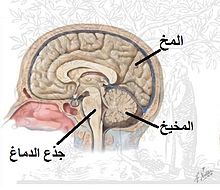
وصف تركيب الدماغ
وبهذه المقالة معلومات أساسية عن الدماغ.
يعلو المخ كلاً من المخيخ وجذع الدماغ، ويلتف حولهما بدرجة ما، ويشكل نحو 85% من الدماغ، ويُعَدُّ الأكثر تعقيداً. وللإنسان مخ متطور النمو، يقوم بتوجيه السمع والنظر واللمس والتفكير والإحساس والكلام والتعلم.
يعلو المخيخ ـ والذي يقارب حجمه حجم البرتقالة ـ جذع الدماغ ويساعد الجسم في الاحتفاظ بتوازنه وينسق بين المعلومات الحسيّة وحركة العضلات.
يشبه جذع الدماغ الساق، ويتصل بالنخاع الشوكي في قاعدة الجمجمة. ويحتوي على العديد من العصبونات التي تتبادل المعلومات الواردة من الحواس. والكثير من العصبونات التي تنظم الوظائف التلقائية، مثل التنفس والنبض القلبي وتوازن الجسم وضغط الدم، توجد في جذع الدماغ.
يتكون النخاع الشوكي من حبل من العصبونات التي تمتد من العنق وتتدلى حتى مايقرب من ثلثي العمود الفقاري، الذي يلتف حوله ويقوم بوقايته. ويحتوي النخاع الشوكي على السبل التي تنقل المعلومات الحسية للدماغ وتلك التي تتبادل أوامر الدماغ مع العصبونات الحركية.
جهاز العصبي المحيطي
يعمل الجهاز العصبي المحيطي على نقل الإشارات والرسائل بين الجهاز العصبي المركزي وأعضاء الجسم المختلفة، ويتكون من اثني عشر زوجاً من الأعصاب تبدأ من الدماغ، وتُسمى: الأعصاب القحفية، بالإضافة إلى واحد وثلاثين زوجاً من الأعصاب التي تبدأ من النخاع الشوكي وتُسمى: الأعصاب النُخَاعية. وتعمل هذه الأعصاب كأسلاك الهاتف، حيث تقوم بنقل الرسائل من كل عَصْبون مستقبل ومستفعل في الجسم وإليه.
الجهاز العصبي الذاتي
يُعدُّ الجهاز العصبي الذاتي جزءاً خاصاً من الجهاز العصبي المحيطي، حيث يعمل على تنظيم كل الوظائف الذاتية (أي التلقائية) في الجسم، مثل التنفس والهضم، دون أي تدخُّل أو تحكم من الدماغ، مما يساعد على الاحتفاظ ببيئة داخلية مستقرة.
وينقسم الجهاز العصبي الذاتي إلى جهازين متخاصمين (أي كل جهاز يحاول أن ينفذ عكس الذي ينفذه الجهاز الآخر) هما: الجهاز الوُدِّي والجهاز اللاوُدِّي.
يلبي الجهاز الودِّي كل احتياجات الجسم خلال حالات الطوارئ وازدياد النشاط. فهو يعمل على ازدياد سرعة ضربات القلب وسريان الدم للعضلات وتوسعة حدقتي العينين. إذا يعمل الودي في حالة القتال أو الهروب (الكر والفر)، والذي يعرف بالإنكليزية: (Fight-or-Flight) ترجمتها الحرفية: (قاتِل أو اهرُب)
أما الجهاز اللاوُدِّي فيقوم، بشكل عام، بإحداث تأثيرات مضادة للجهاز الودِّي. فمن تأثيراته مثلاً، إبطاء ضربات القلب وتوجيه سريان الدم من العضلات إلى المعدة والأمعاء، وتضييق حَدَقَتي العينين. إذا يعمل اللاودي في حالة الراحة أو الاسترخاء، والذي يعرف بالإنكليزية: (rest-and-digest) وترجمتها الحرفية: (استرخِ واهضُم)
أما الموازنة بين الجهازين، فيقوم بها الجهاز العصبي المركزي.
أجزاء العصبون
الهيكلُ النموذجي للخلية العصبية (العصبون) العصبون 
زائدة شجرية
الجسم
المحور
النواة
عقدة رانفييه
نهاية المحور
خلية شوان
غمد الميالين
يتكون العصبون من ثلاثة أجزاء أساسية هي: الجسم الخَلَوي والمحوار (المحور العصبي) والتغصنات. ويغطي كل الخلية غشاء عصبي رقيق.
الجسم الخلوي
يشبه الجسم الخلوي كرة صغيرة قطرها 0,25ملم، ويعمل على استقبال وإرسال الدفعات العصبية وتصنيع البُروُتينات واستخدام الطاقة للمحافظة على الخلية العصبية ونموها.
تتمركز معظم الأجسام الخلوية للعصبونات داخل الجهاز العصبي المركزي، حيث تتحد الرسائل الواردة وتُبَث الرسائل الصادرة. أما تلك الموجودة خارج الجهاز العصبي المركزي، فتتجمع في حزم تسمى العقد العصبية، مثل تلك الخاصة بالجهاز العصبي التلقائي.
المحور
ويسمى أيضاً الليف العصبي، ويشكل امتداداً أنبوبياً للجسم الخلوي للعصبون. وله العديد من التفرعات التي تمكنه من الاتصال بما يقرب من ألف عصبون آخر. وهو متخصص في نقل الرسائل.
يبلغ طول المحوار داخل الجهاز العصبي المركزي أقل من مليمتر واحد، بـينما يزيد عن ذلك في الجهاز العصبي المحيطي، إذ يصل طول بعض المحاوير الممتدة من النُخاع الشوكي إلى عضلات القدمين إلى 75-100سم.
أما الأعصاب فما هي إلا تجمعات لمحاوير عصبونات حركية أو حسية أو لكليهما (عصبونات مختلطة) معًا، التصقت مع بعضها البعض مكونة ذلك الشكل الحبلي.
يغطي غمد مصنوع من مادة دهنية بيضاء تسمى الميالين (نخاعين) بعض المحاوير، حيث تساعد على سرعة انتقال الدفعات العصبية عبرها، كما تساعد على التمييز بين المادة الرمادية والمادة البيضاء في الجهاز العصبي. وتتكون المادة الرمادية من محاوير غير مغطاة بالميلين وأجسام خلوية عصبونية، بينما تتكون المادة البيضاء من محاوير مغطاة بالميلين. وتصنع مادة الميلين في خلايا شوان في الجهاز العصبي المحيطي، بينما تقوم الخلايا الدبقية بتصنيعها في الجهاز العصبي المركزي.
التغصُنات
تتفرع من كل جسم خَلَوي نحو ستة أفرع في شكل قنوات أسطوانية، تُسمى التغصنات. ويبلغ طولها نصف ملم وسُمكها ضعفي سُمك المحوار أو ثلاثة أضعافه. تُعَدُّ التغصنات أجسامًا متخصصة في استقبال الدُفعات الواردة من محاوير أخرى، ويفصل بينهما فراغ ضيق يُسمى الفَلُح المَشْبَكي الذي تعبر خلاله الدُفعات. وتسمى أماكن التقاء العصبونات المشابك.
مسارات الرسائل العصبية
السبل البسيطة
يعمل الجهاز العصبي عبر سُبل محددة وثابتة بين العصبونات تسمى الدارات العصبية. ومن أبسطها ما يسمى بالمُنْعَكس، وهي استجابة تلقائية لا إرادية لأحد المنبهات لا يتدخل فيها الدماغ. ويربط المنعكس بين عَصْبونات مُستَقْبلة ومستفعلة ويمر عبر النُّخاع الشوكي.
ومن أبسط هذه المنعكسات مُنْعكَسُ الركبة الذي يمكن مشاهدته بعد طرق خفيف على الوتر تحت الرضَفَة. فالطّرْق يؤدي إلى تقلص العضلة هناك وتنبيه بعض المستقبلات وانبثاق دفعة عصبية، تنتقل عبر عَصْبون حسي من خلال محوار إلى النُخاع الشوكي، ومن ثَمّ ـ عبر مشبك ـ إلى حد العَصبونات الحركية، حيث يتم تكوين دُفعة عصبية أخرى تنتقل عبر المحوار لأحد العُصبونات الحركية ليتم إرجاعها للعضلة التي تنقبض خلاياها مُحدثة نفضًا للساق.
السُبل المعقّدة
هنالك العديد من المنعكسات المعقدة، حيث تدخل إحدى عَصبونات الترابط بين العَصبونات الحسية والحركية. وقد يتصل عَصْبون الترابط بمجموعة من السبل العصبية المعقدة التي قد تصل إلى الدماغ. ومن هذه المنعكسات، الانسحاب من أحد المنبهات المؤلمة، مثل ما يحدث عندما يضغط شخص ما بقدمه الحافية على جسم حادّ. ففي هذه الحالة نشاهد استجابة فورية برفع القدم، وفي نفس الوقت ينبِّه بعض عَصبونات الترابط عضلات الرِّجل الأخرى لتحافظ على توازن الجسم. وإضافة لهذا يتم تنبيه بعض السبل العصبية الواصلة للدماغ ليعي الإنسان ما حدث له.
ولا تستطيع المنعكسات بمفردها احتواء كل أفعال الإنسان وتفسيرها، ويمكن للإنسان وبعض الحيوانات تعلَّم أنماط جديدة من السلوك. فمثلاً، تنتقل حركات العضلات الإرادية المطلوبة لاكتساب خبرات جديدة، عبر مجموعة من السبل العصبية المعقدة التي تمتد من الدماغ إلى جميع أعضاء الجسم. فبعض الأفعال المعقدة مثل قيادة الدراجة أو المشي يمكن التدرُّب عليها، وتعلمها، ومن ثم أداؤها دون أي تحكم واعٍ مستديم.
كيفية نقل العصبونات للدُفعات العصبية
في خلال القرن التاسع عشر الميلادي، اكتشف العلماء علاقة الشحنات الكهربائية بالدفعات العصبية، وظنوا أن الدفعة العصبية ماهي إلا تيار كهربائي يسري عبر الأعصاب. وفي بداية القرن العشرين عرف الباحثون قدرة بعض الأيونات داخل العصبونات وخارجها على إحداث شحنات كهربائية كامنة، وكذلك اكتشف وجود بعض المسام في أغشية الخلايا العصبية، تسمح بمرور بعض المواد المعينة من خلالها. ولذلك اعتقد العلماء بأن الدفعات العصبية عمليات كهروكيميائية تتحكم فيها أغشية الخلايا العصبية، ولذلك من هذه التجارب انبثق مجال الفيزيولوجيا الكهربية.
وفي خلال الثلاثينيات من القرن العشرين، طَوّرَ العلماء بعض الطرق لاختبار نظرية الغشاء في التوصيل العصبي، وهي نظرية مقبولة لتفسير كيفية نقل العُصبونات للدفعات العصبية.
بدء الدُفعة العصبية. يحتوي غشاء الخلية العصبية على جُزيئات بروتينية خاصة تتحكم في فتح مسامه وإغلاقها. وخلال فترة سكونه يتم تخفيض مستوى أيونات الصوديوم وزيادة مستوى أيونات البوتاسيوم وبعض الأيونات العضوية السالبة داخل الخلية مقارنة بما يحيط بها من سوائل، ومن ثم تزداد سلبية داخل العصبون. ويطلق على الغشاء العصبوني في هذه الحالة اسم الغشاء المُستَقطب. ويسمى فرق الجهد عبر الغشاء اسم الكَامن الساكن.
وعند تنبيه العَصبون بأحد المنبهات الكيميائية أو الكهربائية أو الآلية تتأثر مسامية الغشاء، ويتغير الجهد الساكن. فهذه المنبهات تفتح مسامات الغشاء وتزيد من دخول أيونات الصوديوم لداخل الخلية، حيث يزداد عدد الشحنات الموجبة، ويحدث ما يسمى بزوال الاسْتِقْطاب.
وعند إزالة استقطاب العَصبون بأحد المنبهات، يبدأ بالنبض ويزداد نشاطه، ومن ثم تبدأ الدفعة العصبية. ويجب أن تكون للمنبه شدة معينة تعرف باسم جهد العتبة.
وتجدر الإشارة إلى أن لكل الدفعات العصبونية نفس الحجم والزمن، بغض النظر عن قوة المنبه للعصبون، وتسمى هذه الظاهرة باسم ظاهرة الكل ـ أو ـ العدم. ويحتمل أن ترجع قدرة إحساس الدماغ بقوة المنبه إلى عدد الألياف العصبية المنبهة وتردُّد الدفعات الناتجة عن المنبه.
التوصيل عبر المحوار. يوجد بداخل المحوار العصبي سائل ذو قدرة على توصيل الشحنات الكهربائية ونقلها في شكل تيار. فعند إزالة الاستقطاب من إحدى مناطق المحوار، تنتشر هذه الإزالة عبر هذا السائل إلى كل المناطق المجاورة في المحوار. وتسمى موجة إزالة الاستقطاب هذه باسم كامن الفعل.
وتجب ملاحظة أنه لو كان العَصبون غير مُغطى بمادة المَيلين لأمكن للدفعات العصبية اكتساح المحوار كله مرة واحدة، كاكتساح النار لفاصمة الانصهار الواقية. ولكن لوجود غطاء الميلين وتقطعه عبر المحوار في مناطق عُقد رانفير، فلا تحدث هذه الدُفعات العصبية إلا في هذه العقد حيث تقفز من عقدة إلى أخرى عبر المحوار.
الانتقال عبر المَشابك. يتم انتقال الدفعات العصبية عبر المشابك بوساطة مواد كيميائية خاصة تسمى الناقلات العصبية. فعند وصول الدفعة للنهاية الطرفية للمحوار تقوم بحفز إفراز إحدى الناقلات العصبية في الفلح المشبكي، ومن ثم تتحرك الناقلة العصبية نحو تغصنات الخلية العصبية المجاورة، وتفتح مسامات غشائها لتتدفق بعض الأيونات إلى داخل الخلية، لتحدث تغييرًا في جهدها يسمى الكامن خلف المشبك.
ينقسم الكامن خلف المشبك إلى نوعين: مُثير أو مُثَبِّط. ويعمل النوع المثير لإحداث فعل كامن آخر في محوار إحدى الخلايا العصبية، بينما يعمل النوع المثبِّط لمنع حدوثه. وتجدر الإشارة إلى عدم قدرة بعض الدفعات العصبية الواصلة إلى المشبك من الوصول إلى العُصبونات المجاورة، مما يعني أن المشابك تعمل على تنظيم مسار تدفقات الدفعات العصبية الثابتة في كل أجزاء الجهاز العصبي.
اضطرابات الجهاز العصبي
تضر بعض الأمراض والإصابات بالجهاز العصبي. ويصعب إصلاح محاوير الجهاز العصبي المركزي بعد تلفها الكبير. ولكن يمكن لبعض الأعصاب في الجهاز العصبي المحيطي استرداد وظيفتها إذا كان الضرر طفيفًا.
تتجمع معظم العَصبونات التي تؤدِّي وظيفة محددة في منطقة واحدة من الدماغ. وبسبب هذا الانتظام التجميعي الذي يسمى توضيع الوظيفة، فإن العطب أو الضرر الجزئي في الدماغ، لا يؤدي إلا لفقدان تلك الوظائف المسؤول عنها ذلك الجزء. ولكن قد يصدف أن تتولى بعض الأجزاء السليمة من الدماغ عمل تلك الأجزاء التالفة مؤدية إلى ما يُسمى باستعادة الوظيفة.
والسكتة الدماغية. من أخطر اضطرابات الجهاز العصبي، وتحدث عندما يتوقف سريان الدم إلى بعض أجزاء الدماغ، مما يؤدي لموت الخلايا العصبية وعدم القدرة ـ الدائمة أو المؤقتة ـ على أداء بعض الوظائف مثل الكلام أو تحريك الأطراف. وقد يموت الإنسان في حالة تلف مراكز التحكم في التنفس أو أية وظيفة حيوية أخرى.
ومن أمراض الجهاز العصبي المعدية الشائعة بعض الإصابات الفيروسية البسيطة التي تستمر لأيام قليلة فقط مسببة الصداع أحيانًا. ولكن هنالك أيضًا بعض الأمراض الخطرة مثل التهاب الدماغ والالتهاب السحائي تسببها بعض البكتيريا، والفيروسات والميكروبات الأخرى.
ويُصاب الجهاز العصبي أيضًا بمرض التصلب المتعدد وهو غير معروف السبب ويؤدي لفقدان الأغشية الميلينية للمحاوير في الجهاز العصبي المركزي، مما يُبطل قدرتها على توصيل الدفعات العصبية بصورة جيدة.
وكذلك يصاب الجهاز العصبي المركزي بمرض الصَّرْع الذي تحدث فيه اختلاجات عضلية قد تكون مصحوبة بتغيير أو فقدان مؤقت للوعي. وتحدث النوبات الصرعية عند انبثاق عدد هائل من الدفعات العصبية من بعض العَصبونات في أحد مناطق الدماغ. ويصف الأطباء بعض الأدوية للتقليل من هذه النوبات أو منعها نهائيًا.
وإضافة لهذا فقد يصاب الجهاز العصبي بمرض شلل الأطفال الذي يسببه فيروس شلل الأطفال. وهو يتلف العَصبونات الحركية في النخاع الشوكي وجذع الدماغ مؤدية بذلك إلى الشلل في بعض الأحيان. ولكن بعد اكتشاف لقاحات هذا المرض وتطويرها قلت الإصابة به.
وتؤدي اضطرابات الجهاز العصبي إلى بعض الأمراض العقلية أو التخلف العقلي.
الجهاز العصبي عند الحيوانات
الحيوانات الفقـارية. تمتلك الحيوانات الفـقارية من ثدييات وأسماك وطيور وزواحف وبرمائيات عَصبوناتٍ وجهازًا عصبيًا، يشبه من حيث الشكل والحجم ذلك الذي لدى الإنسان. ويدل كبر حجم جزء ما من الدماغ على أهمية ذلك الجزء للحيوان. فمثلاً نلاحظ أن منطقة الشّم في الكلاب، تحتل مكانة أكبر من مثيلتها عند الإنسان، ولكن، الإنسان يتميز بامتلاكه لقشرة مخ ـ الجزء الخارجي من الدماغ ـ كبيرة ومتطورة مسؤولة عن تنسيق المهارات المعقدة، مثل التحكم في حركة الجسم وتعلم اللغات. و ذلك راجع إلى طريقة عيشه خلال مراحل تطوره إذ لم يكن ينجو خلال عمليات الصيد المعقدة و طرق الحياة الصعبة خاصة أمام عدم توفره على مؤهلات طبيعية أخرى إلا أصحاب الذكاء العالي و بالتالي و بالانتخاب الطبيعي انتقلت الجينات الأكثر ذكاءا و التي لم ينج غيرها و تطورت عبر التاريخ فالٱنسان البدائي كان حجم عقله لا يتعدى حجمه ثلثي حجمه الحالي و بالتالي فلم يكن بالذكاء الذي هو عليه اليوم.
الحيوانات اللافقارية. تمتلك الحيوانات اللافقارية المتعددة نوعاً ما من الأجهزة العصبية ذات عصبونات كبيرة مقارنة بتلك التي عند الإنسان. فمثلاً تمتلك الحيوانات البسيطة، مثل الهيدرا جهازاً عصبياً يتكون من شبكة عصبية تنتشر في كل خلايا الحيوان. ولا يمكن التمييز بين المحاوير والتغصنات، ولذلك تنتشر الدفعات العصبية بصورة شاملة في كل الحيوان عند بدئها من موضع التنبيه.
ومن ناحية أخرى تمتلك الديدان والحشرات جهازا عصبياً مركزياً معقداً يتكون من عَصبونات كثيفة مُشكّلة ما يُسمى: الحبل العصبي المليء بالعُقد ذات القدرة على تنظيم أنشطة هذه الحيوانات وتنسيقها.
وإضافة لهذا نلاحظ في مقدمة الحيوان وجود تجمعات من العقد تمثل ما يُسمى الدماغ البدائي. وللحشرات كذلك تجمعات عُقدية في الصدور مسؤولة عن تنسيق حركتها. ومن ناحية عامة تتشابه آليات حدوث الدُفعات العصبية والكوامن المشبكية في كل من الإنسان والأنواع المتقدمة من الحيوانات اللافقارية.
محتويات
- 1 آلية عمل الجهاز العصبي
- 2 أقسام الجهاز العصبي
- 2.1 الجهاز العصبي المركزي
- 2.2 جهاز العصبي المحيطي
- 3 أجزاء العصبون
- 3.1 الجسم الخلوي
- 3.2 المحور
- 3.3 التغصُنات
- 4 مسارات الرسائل العصبية
- 4.1 السبل البسيطة
- 4.2 السُبل المعقّدة
- 5 كيفية نقل العصبونات للدُفعات العصبية
- 6 اضطرابات الجهاز العصبي
- 7 الجهاز العصبي عند الحيوانات
- 8 انظر أيضا
- 9 مراجع